Webinar del 3 de junio | Decisiones clave sobre evidencia clínica para el mercado de dispositivos médicos de EE. UU. y la UE

Lamentablemente no somos totalmente compatibles con su navegador. Si tiene la opción, actualice a una versión más reciente o utilice Mozilla Firefox, Microsoft Edge, Google Chrome o Safari 14 o posterior. Si no puede y necesita ayuda, envíenos sus comentarios.
Agradeceríamos sus comentarios sobre esta nueva experiencia.Díganos qué piensase abre en una nueva pestaña/ventana
¿Le falta información crítica para el cumplimiento y el desarrollo de dispositivos médicos? Embase proporciona búsquedas bibliográficas específicas sobre dispositivos médicos a través de una amplia cobertura de contenido, indexación precisa y términos específicos del dispositivo.
Póngase en contacto con nosotros para obtener más información sobre Embase para dispositivos médicos


Embase cuenta con las herramientas de investigación, evidencia y monitoreo de literatura de dispositivos médicos para ayudarlo a:
Desarrollar y validar nuevos conceptos
Cumplir con las regulaciones de dispositivos médicos
Preparar informes de evaluación clínica para la aprobación de comercialización de CE
Llevar a cabo la vigilancia posterior a la comercialización

Embase elimina la molestia de crear las complejas cadenas de búsqueda necesarias para búsquedas de alta recuperación y alta precisión. Un formulario de búsqueda de dispositivos médicos y términos preestablecidos eliminan las conjeturas de la búsqueda.

Nuestro equipo indexa manualmente los artículos de texto completo, por lo que puede buscar por dispositivo, concepto, fabricante, procedimiento, nombre comercial del dispositivo, términos de la Nomenclatura Global de Dispositivos Médicos (GMDN) aprobados por la FDA y más.
Las alertas por correo electrónico garantizan que reciba la información más reciente publicada, incluidos los preprints y las actas de conferencias.

La falta de una búsqueda de SOTA es una de las principales razones de los hallazgos de no conformidad con MDR/IVDR.
Utilice el comando de búsqueda de Embase para mantenerse al día con el contenido relevante de SOTA de acuerdo con la guía regulatoria.
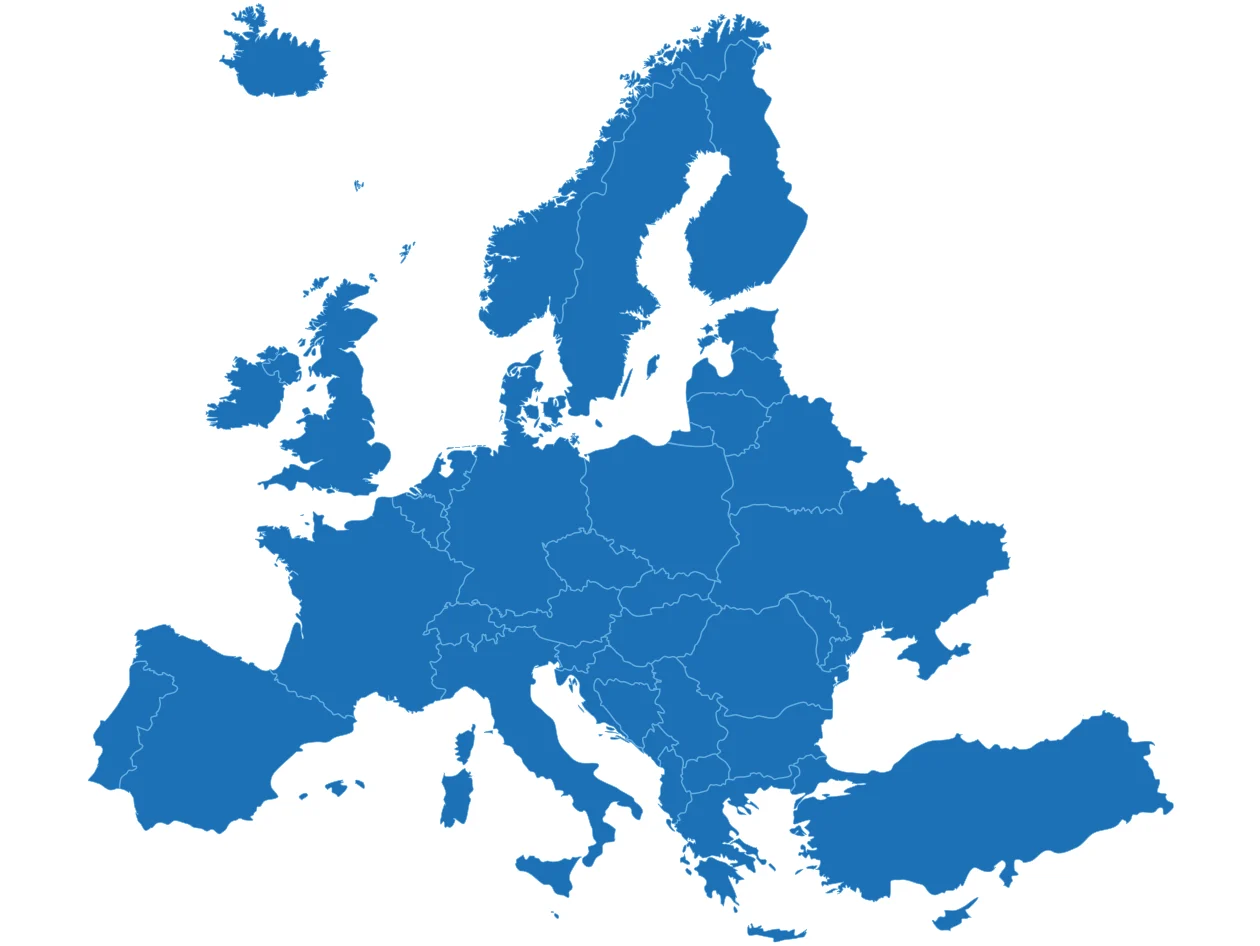
Para cumplir con el MDR, las bases de datos deben mostrar un alcance europeo suficiente.
Embase cubre todo el contenido de MEDLINE y tiene una cobertura única para Europa, incluidos resúmenes de congresos y revistas europeas.
Una de las cosas más sorprendentes de Embase es que todo el artículo está indexado por términos y nombres de productos. Para los productos sanitarios, poder localizar información sobre un producto específico es una gran ventaja».
Dawn McMillen
Supervisor de recursos de la biblioteca en Stryker Orthopedics
