Dec. 3 WEBINAR | Leveraging Embase AI in life science research with Dr. Vassiki Sanogo and Regina Maxwell, MLIS

Votre navigateur n’est malheureusement pas entièrement pris en charge. Si vous avez la possibilité de le faire, veuillez passer à une version plus récente ou utiliser Mozilla Firefox, Microsoft Edge, Google Chrome, ou Safari 14 ou plus récent. Si vous n’y parvenez pas et que vous avez besoin d’aide, veuillez nous faire part de vos commentaires.
Nous vous serions reconnaissants de nous faire part de vos commentaires sur cette nouvelle expérience.Faites-nous part de votre opinionS’ouvre dans une nouvelle fenêtre
Il vous manque des informations essentielles pour la conformité et le développement des dispositifs médicaux ? Embase fournit des recherches ciblées dans la littérature sur les dispositifs médicaux grâce à une large couverture de contenu, une indexation précise et des termes spécifiques aux dispositifs.
Contactez-nous à propos d’Embase pour les dispositifs médicaux


Embase dispose d’outils de recherche sur les dispositifs médicaux, de données probantes et de suivi de la littérature pour vous aider à :
Développer et valider de nouveaux concepts
Respecter la réglementation relative aux dispositifs médicaux
Préparer les rapports d’évaluation clinique pour l’approbation de la mise sur le marché de la CE
Effectuer une surveillance post-commercialisation

Embase simplifie la création des chaînes de recherche complexes nécessaires à des recherches de haute précision et de rappel. Un formulaire de recherche de dispositifs médicaux et des termes prédéfinis éliminent les conjectures de la recherche.

Notre équipe indexe manuellement les articles en texte intégral, ce qui vous permet d’effectuer une recherche par dispositif, concept, fabricant, procédure, nom commercial de l’appareil, termes de la nomenclature mondiale des dispositifs médicaux (GMDN) approuvés par la FDA, etc.
Les alertes par e-mail vous permettent de recevoir les dernières informations publiées, y compris les prépublications et les actes de conférences.

L’absence d’une recherche SOTA est l’une des principales raisons des constatations de non-conformité MDR/IVDR.
Utilisez la commande de recherche d’Embase pour vous tenir au courant du contenu SOTA pertinent conformément aux directives réglementaires.
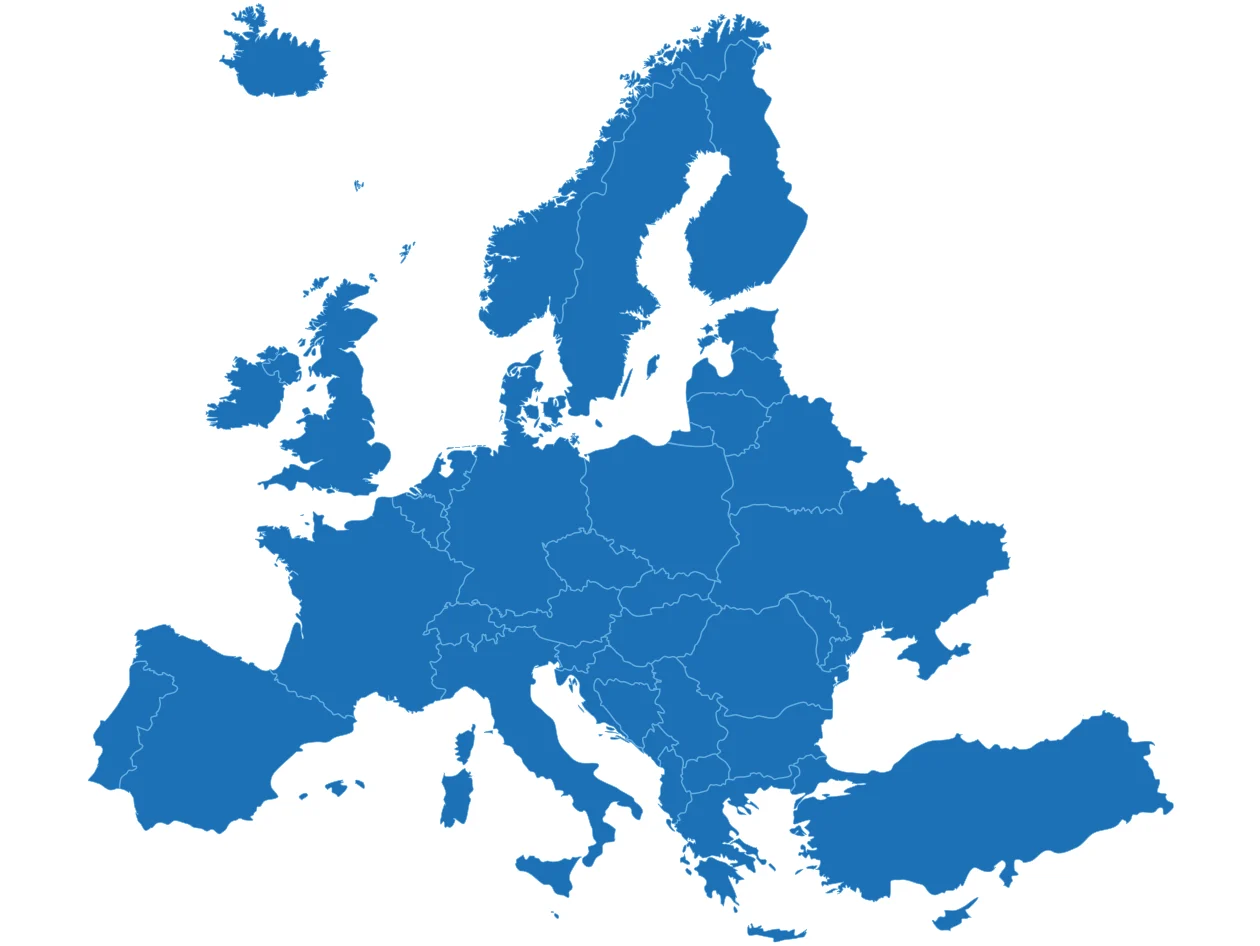
Pour être conformes au MDR, les bases de données doivent avoir une portée européenne suffisante.
Embase couvre tout le contenu de MEDLINE et offre une couverture unique pour l’Europe, y compris les résumés de conférences et les revues européennes.
L’un des aspects les plus formidables d’Embase est que l’article entier est indexé sur les termes et les noms de produits. Pour les dispositifs médicaux, la possibilité de localiser des informations sur un produit spécifique est un énorme avantage.
Dawn McMillen
Superviseure des ressources documentaires de Stryker Orthopedics
