Vereinfachen Sie regulatorische Recherchen mit PharmaPendium AI

Leider unterstützen wir Ihren Browser nicht vollständig. Wenn Sie die Möglichkeit dazu haben, nehmen Sie bitte ein Upgrade auf eine neuere Version vor oder verwenden Sie Mozilla Firefox, Microsoft Edge, Google Chrome oder Safari 14 bzw. eine neuere Version. Wenn Sie nicht dazu in der Lage sind und Unterstützung benötigen, senden Sie uns bitte Ihr Feedback.
Wir würden uns über Ihr Feedback zu diesen neuen Seiten freuen.Sagen Sie uns, was Sie denkenWird in neuem Tab/Fenster geöffnet
PharmaPendium kombiniert beispiellose Zulassungs- und Arzneimitteldaten mit Volltextsuche und Vorhersagewerkzeugen. Reduzieren Sie Tierversuche und bringen Sie Medikamente schneller auf den Markt mit PharmaPendium.

Von größter Bedeutung ist die Rolle von PharmaPendium bei der Bereitstellung von Informationen zu klinischen unerwünschten Ereignissen, wodurch die Identifizierung zugrunde liegender Toxizität in nichtklinischen Studien ermöglicht wird.

Guy Bouvier, PhD, ERT
Direktor, Toxikologie und Produktsicherheit bei Groupe Pierre Fabre
Die Vorhersage pharmakokinetischer Arzneimittelwechselwirkungen mit maximaler Relevanz, Präzision und Reaktionsgeschwindigkeit ist entscheidend. DDIRC ermöglicht schnelle Antworten und damit Entscheidungen zu Interaktionsrisiken.
Yannick Parmentier
Leiter der biopharmazeutischen Forschungsabteilung bei Servier
Mit PharmaPendium erhalte ich Informationen darüber, wie etwas gemessen wurde, und mit einem Klick sehe ich, aus welchem Quelldokument es stammt — all das ist sehr wichtig, um robuste und fundierte Modelle zu erstellen.
Senior Modeler
Novartis

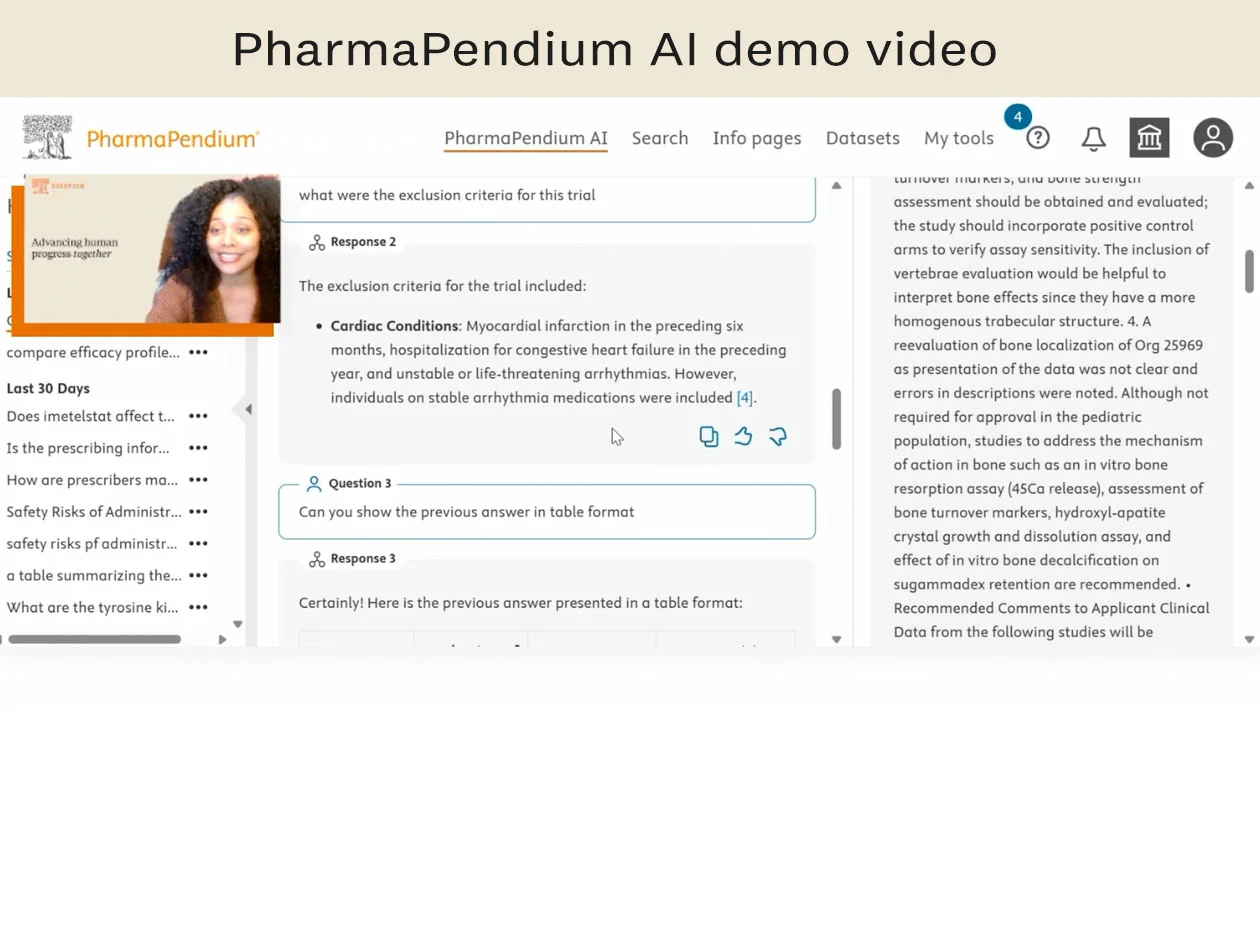
Um die besten Kandidaten voranzubringen, möchten Sie bessere Leistung belegen. PharmaPendium bietet benutzerfreundliche Tools zur Analyse von Sicherheits‑, Verabreichungs‑ und Wirksamkeitsdaten.
Sagen Sie Arzneimittel‑Arzneimittel‑Interaktionen mit Zuversicht voraus. Bewerten Sie das Risiko von Off‑Target‑Nebenwirkungen (Safety Margin Tool).
Greifen Sie mit einem translationalen Blick über Präklinik, Klinik und Post‑Market auf Daten zu, darunter:
Präklinische und klinische Sicherheit
Tiermodelle
Unerwünschte Ereignisse (MedDRA)
Pharmakokinetische Parameter
Metabolismus und Transport
Klinische Studien und Endpunkte
Post‑Market‑Berichte (FAERS)

Reduzieren Sie regulatorische Schleifen und vermeiden Sie Ablehnungen mit PharmaPendium.
Entdecken Sie vollständige regulatorische Dossiers von EMA und FDA sowie Unterlagen der FDA Advisory Committees
Durchsuchen Sie globale Leitlinien von FDA, EMA und ICH für konforme Entscheidungen in der Arzneimittelentwicklung
Analysieren Sie frühere Einreichungen und nutzen Sie Präzedenzfälle, um Anforderungen der Behörden vorherzusagen
Vergleichen Sie Ihre Wirkstoffkandidaten mit zugelassenen oder zurückgezogenen Arzneimitteln mit gleichem Wirkmechanismus
Reagieren Sie schnell auf regulatorische Fragen mit Vergleichsdaten aus FDA/EMA-Zulassungsunterlagen

Der in Zusammenarbeit mit Pfizer entwickelte Tox Navigator umfasst Toxizitätsdaten aus regulatorischen Dokumenten und wissenschaftlichen Artikeln.
Zur Unterstützung der 3Rs und der Bewertung der Patientensicherheit hilft Ihnen der Tox Navigator dabei:
Tierdosen in humankompatible Dosen (HEDs) umzurechnen
Vorhandene Daten zu nutzen, um die Zahl der Tierversuche zu reduzieren und effizientere Studien zu konzipieren
Unerwünschte Arzneimittelreaktionen artspezifisch zu untersuchen
In-silico-Modelle und andere tierversuchsfreie Testmethoden zu integrieren
Forschungsaktivitäten zu optimieren, indem Sie sich auf Kandidaten mit günstigem Sicherheitsprofil konzentrieren

Bringen Sie Ihre Forschung voran – mit PharmaPendium von Elsevier und einem Portfolio an Lösungen für die pharmazeutische F&E.
Innovieren Sie mit Vertrauen, unterstützt durch:
verlässliche Qualitätsinformationen, von regulatorischen Daten bis zu peer-reviewter wissenschaftlicher Literatur
innovative Technologien für Datentransformation sowie Analyse- und Prognosetools
Fach- und Data-Science-Expertise, um komplexe Probleme mit Datenlösungen für die F&E zu lösen
Informationsintegrität ist entscheidend für Ihren Fortschritt. Entdecken Sie verlässliche Daten und Tools, die wichtige Erkenntnisse liefern.
Lassen Sie uns Fortschritt gemeinsam gestalten.
... PharmaPendium zeichnet sich durch das Abrufen spezifischer Toxizitätsbeobachtungen in Zulassungsdokumenten aus, die nach Arzneimittel und Spezies kategorisiert sind.
Guy Bouvier, PhD, ERT
Direktor, Toxikologie und Produktsicherheit bei Groupe Pierre Fabre
Die kontinuierliche Weiterentwicklung und Verbesserung von PharmaPendium erfolgt seit 17 Jahren in Zusammenarbeit mit der FDA sowie mit führenden Pharmapartnern wie Novartis, Sanofi, Merck, Servier und Boehringer Ingelheim.
Folgende Personen setzen PharmaPendium ein:
Toxikolog*innen und Sicherheitspharmakolog*innen
DMPK-Spezialist*innen
Klinische Forscher*innen
Expert*innen für regulatorische Angelegenheiten
Globale Expert*innen für Patientensicherheit
Datenwissenschaftler*innen
PharmaPendium bietet Ihnen einzigartige Inhalte − an einem zentralen Ort. Zu den Datenquellen von PharmaPendium gehören:
Vollständige FDA-Zulassungspakete
Vollständige EMA-Zulassungsdokumente
Dokumente des FDA-Beratungsausschusses
FDA Adverse Event Reporting System (FAERS)
FDA Classic Collection (von 1938 bis 1991)
DESI (Drug Efficacy Study Implementation)-Dokumente
Meyler's, 16. Auflage
Mosby's Drug Consult™️
Wissenschaftliche Artikel
Wir extrahieren, organisieren, verbinden und aktualisieren kontinuierlich eine Vielzahl von Daten in PharmaPendium.
Holen Sie sich die neuesten Inhaltsstatistikenopens in new tab/window für PharmaPendium.
PharmaPendium enthält Sicherheits-, PK-, MET-, Wirksamkeits-, Aktivitäts-, FAERS- und Arzneimitteldaten sowie Zulassungspakete und Dokumente der FDA und EMA.
Durch die Kombination von PharmaPendium und Embase können Sie nach zusätzlichen Indikationen für die Umnutzung nicht zugelassener oder zugelassener Medikamente suchen. Dank der breiten Datenvielfalt in Embase und PharmaPendium können Sie nach relevanten klinischen Studien und Daten suchen, um die Anforderungen an das Design klinischer Studien zu prognostizieren und Risiken zu mindern. Zusätzlich zu den Daten zu zugelassenen Medikamenten in PharmaPendium bietet Embase Informationen zu nicht zugelassenen Medikamenten. Embase deckt mehr als 8.500 Wissenschaftsjournals und Millionen von Abstracts von 11.500 Konferenzen weltweit ab.
