규제 검색을 PharmaPendium AI로 간소화하세요

귀하의 브라우저가 완벽하게 지원되지 않습니다. 옵션이 있는 경우 최신 버전으로 업그레이드하거나 Mozilla Firefox, Microsoft Edge, Google Chrome 또는 Safari 14 이상을 사용하세요. 가능하지 않거나 지원이 필요한 경우 피드백을 보내주세요.
이 새로운 경험에 대한 귀하의 의견에 감사드립니다.의견을 말씀해 주세요새 탭/창에서 열기
자신 있게 발견, 혁신 및 개발하려면 고품질 데이터가 필요합니다. PharmaPendium은 비교할 수 없는 규제 및 약물 데이터를 전체 텍스트 검색 및 예측 도구와 결합합니다. PharmaPendium으로 동물 실험을 줄이고 약물을 더 빠르게 출시하십시오.

가장 중요한 것은 PharmaPendium이 임상 이상반응에 대한 정보를 제공하여 비임상 연구에서 기저 독성을 식별할 수 있게 해 준다는 점입니다.

Guy Bouvier, PhD, ERT
Groupe Pierre Fabre의 독성학 및 제품 안전 디렉터
최대한의 관련성, 정확성, 대응 속도로 약동학적 약물-약물 상호작용을 예측하는 것은 필수적입니다. DDIRC는 빠른 응답을 가능하게 하며, 따라서 상호작용 위험에 대한 빠른 의사결정을 지원합니다.
Yannick Parmentier
Servier의 생물의약 연구 부서장
PharmaPendium을 사용하면 그것이 어떻게 측정되었는지에 대한 정보를 얻을 수 있고, 클릭 한 번으로 어떤 원문 문서에서 나온 것인지도 확인할 수 있습니다. 이 모든 것은 견고하고 탄탄한 모델을 구축하는 데 매우 중요합니다.
수석 모델러
Novartis

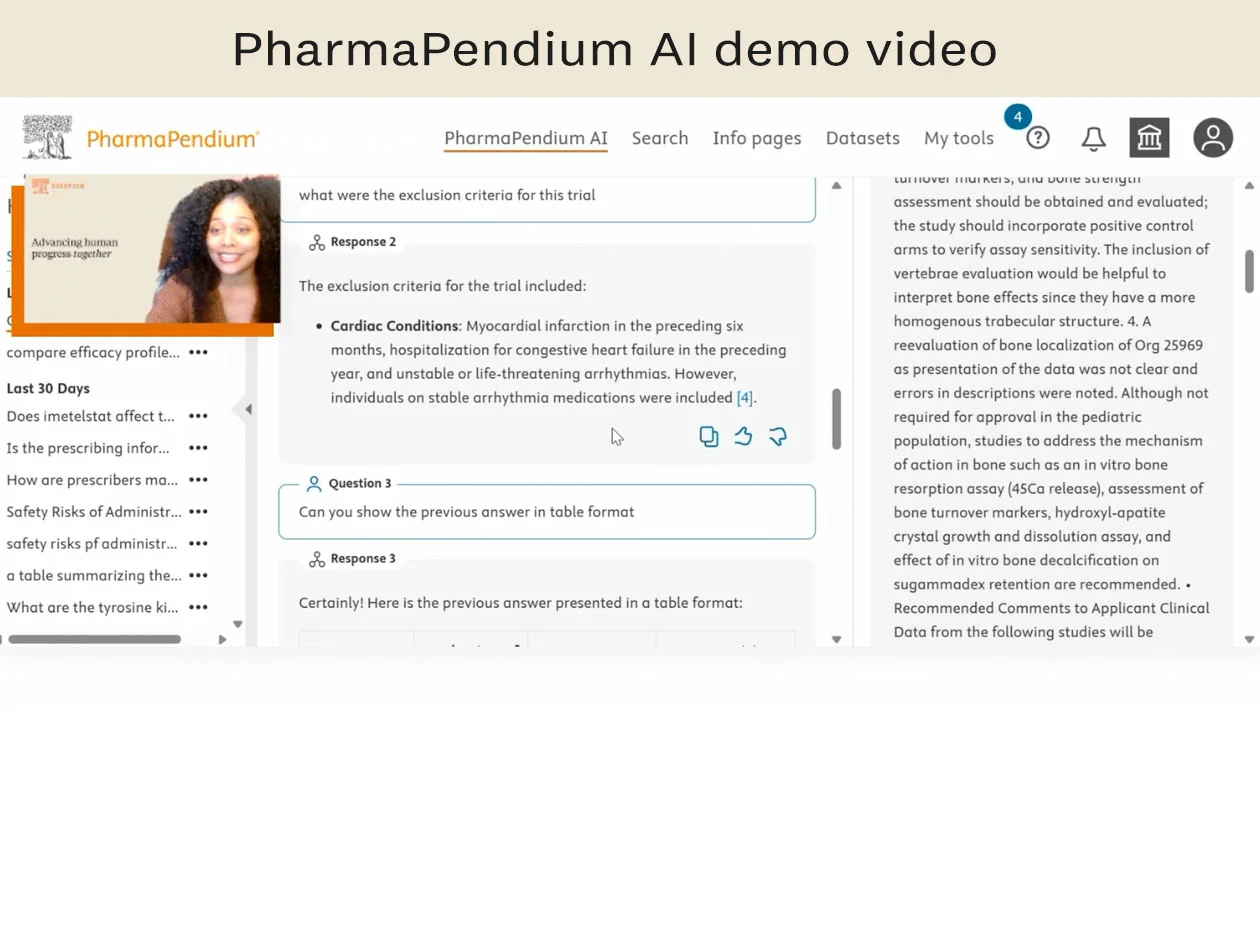
최고의 약물 후보를 발전시키려면 더 나은 성능을 입증하고 싶습니다. PharmaPendium에는 안전성, 전달 가능성 및 효능 데이터를 분석하는 데 도움이 되는 사용자 친화적인 도구가 있습니다.
약물-약물 상호작용을 자신 있게 예측
표적 외 약물 부작용 위험 예측(안전 여유)
다음을 포함하여 전임상, 임상 및 시판 후 전반에 걸친 번역 보기로 데이터에 액세스합니다.
전임상 및 임상 안전성
동물 모델
부작용(MedDRA)
약동학 매개변수
신진대사와 수송
임상 시험 및 종점
시판 후 보고서(FAERS)

PharmaPendium을 통해 규제 주기를 최소화하고 승인 실패를 방지하십시오.
EMA 및 FDA의 전체 규제 패키지와 FDA 자문 위원회 회의 문서 알아보기
FDA, EMA 및 ICH의 글로벌 규제 지침을 검색하여 규정 준수 의약품 개발 의사결정을 지원하세요
이전 규제 제출을 살펴보고 선례를 통해 기관의 요구 사항을 예측합니다.
약물 후보와 동일한 작용 메커니즘을 가진 승인 및 철회 약물에 대한 벤치마킹
FDA/EMA 의약품 승인 및 검토 문서의 비교 데이터를 사용하여 규제 질문에 신속하게 대응

Pfizer와의 협업으로 개발된 Tox Navigator에는 규제 문서와 과학 논문의 독성 데이터가 포함됩니다.
3Rs와 환자 안전성 평가를 지원하는 Tox Navigator는 다음을 가능하게 합니다:
동물 투여량을 인체 상응 용량(HED)으로 환산
기존 데이터를 활용해 동물실험 수를 줄이고 더 효율적인 연구를 설계
종 간 이상 약물반응 조사
in silico 모델과 기타 비동물 시험 방법 통합
안전성 프로파일이 우수한 후보에 집중해 연구 효율을 최적화

Elsevier의 PharmaPendium과 제약 R&D용 솔루션 포트폴리오로 연구를 진전시키세요.
다음을 바탕으로 확신 있게 혁신하세요:
규제 데이터부터 동료심사 과학 문헌까지 아우르는 신뢰할 수 있는 고품질 정보
데이터 전환과 분석· 예측 도구를 구동하는 혁신 기술
R&D를 위한 데이터 솔루션으로 복잡한 문제를 해결하는 도메인 전문성과 데이터 과학 역량
정보의 무결성은 진전을 이루는 데 필수적입니다. 핵심 인사이트를 제공하는 신뢰할 수 있는 데이터와 도구를 확인하세요.
함께 진전을 만들어 갑시다.
... PharmaPendium은 약물 및 종별로 분류된 승인 문서에서 특정 독성 관찰을 검색하는 데 탁월합니다.
Guy Bouvier, PhD, ERT
Groupe Pierre Fabre의 독성학 및 제품 안전 디렉터
PharmaPendium은 FDA와 17년간 협력해 지속적으로 개발·개선되어 왔으며, Novartis, Sanofi, Merck, Servier, Boehringer Ingelheim 등 주요 제약 파트너와도 협업해 왔습니다.
아래 논문은 여러 조직이 워크플로우에서 PharmaPendium을 어떻게 활용하고 있는지 보여줍니다. 해당 내용은 정보 제공 목적으로만 제공되며, 이를 보증하거나 지지하는 것은 아닙니다.
Machine learning models for human in vivo pharmacokinetic parameters with in-house validationopens in new tab/window, Molecular Pharmaceutics AstraZeneca는 PharmaPendium 데이터를 사용해 인체 in vivo PK 매개변수에 대한 머신러닝 모델을 구축했습니다.
Drug interaction with UDP-Glucuronosyltransferase (UGT) enzymes is a predictor of drug-induced liver injuryopens in new tab/window, Hepatology FDA는 PharmaPendium의 DILI 데이터를 사용해 UDP-Glucuronosyltransferase(UGT) 효소와의 약물 상호작용이 약물 유발 간 손상의 예측 인자임을 확인했습니다.
PharmaPendium 사용 대상:
독성학자 및 안전성약리학자
DMPK 전문가
임상 연구자
규제 업무 전문가
글로벌 환자 안전 전문가
데이터 과학자
PharmaPendium은 모든 고유한 콘텐츠를 한곳에서 제공합니다. PharmaPendium 데이터 출처는 다음과 같습니다:
전체 FDA 승인 패키지
전체 EMA 승인 문서
FDA 자문위원회 문서
FDA Adverse Event Reporting System (FAERS)
FDA 클래식 컬렉션(1938-1991)
DESI(Drug Efficacy Study Implementation) 문서
Meyler's 16th Edition
Mosby's Drug Consult™️
과학 논문
PharmaPendium에서는 다양한 데이터를 추출, 구성, 연결하고 지속적으로 업데이트합니다.
최신 PharmaPendium 콘텐츠 통계opens in new tab/window를 확인하세요.
PharmaPendium에는 안전성, PK, MET, 유효성, 활성, FAERS 및 약물 데이터와 FDA 및 EMA의 승인 패키지 및 문서가 포함됩니다.
PharmaPendium과 Embase를 함께 사용하면 미승인 또는 승인 약물의 재창출을 위한 추가 적응증을 찾을 수 있습니다. Embase와 PharmaPendium의 폭넓은 데이터를 바탕으로 임상시험 설계 요건을 예측하고 위험을 완화하는 데 도움이 되는 관련 임상 연구와 데이터를 찾을 수 있습니다.
PharmaPendium의 승인 약물 데이터에 더해 Embase는 미승인 약물 정보도 제공합니다. Embase는 전 세계 11,500개 학회의 수백만 건 초록과 8,500종이 넘는 과학 저널을 포괄합니다.
